მკითხველის არჩევანი
პოპულარული სტატიები
გამარჯობა ყველას! ბევრმა იცის, რომ ოქსალური მჟავა იწვევს თირკმლის ქვების წარმოქმნას. მაგრამ, რა სახის ნივთიერებაა იგი და სად არის ის და როგორ გამოიყენება, ბევრმა არ იცის. აქედან გამომდინარე, შემეცნებითი თვალსაზრისით, ეს სტატია ამის შესახება.
გერმანელმა ქიმიკოსმა ფრიდრიხ ვოლერმა 1824 წელს პირველად მოახდინა ოქსილის მჟავის სინთეზირება. ოქსალიუმის მჟავა (სამეცნიერო სახელი ეთანანდიუმის მჟავაა), მიეკუთვნება ორგანული მჟავების ჯგუფს. ბუნებაში, ოქსილის მჟავა გვხვდება თავისუფალ სახელმწიფოში და კალციუმის და კალიუმის ოქსალატების სახით.
ცოტა რამ oxalic მჟავის ქიმიური და ფიზიკური თვისებების შესახებ.
ოქსალური მჟავა არის კრისტალური, ჰიგიროსკოპიული, უფერო ნივთიერება, უსუნო. იგი ნაწილობრივ ხსნადია ალკოჰოლში (ეთანოლი), წყალში. ქმნის ოქსილის მჟავას დიჰიდრატს.
ოქსილის მჟავა
ოქსილის მჟავის მიღება:
ჩვენ ვიცით, რომ ადამიანის ფიზიკური მდგომარეობა დიდწილად არის დამოკიდებული კუნთების და ნერვების სწორად მუშაობაზე. სისხლის მიმოქცევის სისტემის, საჭმლის მომნელებელი ტრაქტისა და ექსკრეციული ორგანოების ფუნქციონირება ხდება პერისტალტიკულ მოძრაობებზე დაყრდნობით, რომლებიც ბუნებრივად ტალღოვანი ხასიათისაა და შედგება კუნთებისა და ნერვების თანმიმდევრული დასვენებისა და შეკუმშვისაგან.ამ პროცესების ეფექტურობა დამოკიდებულია მათ ფიზიკურ მდგომარეობაზე.
კუნთების და ნერვების მუშაობის კარგი სტიმულაციაა ოქსილის მჟავა.
უნდა გვახსოვდეს, რომ ჩვენს ორგანიზმში სასიცოცხლო პროცესები აქტიური და ცოცხალი იქნება, თუ ორგანოების ქსოვილები და უჯრედები ახალგაზრდა და ჯანმრთელია. თუ ჩვენი ორგანოების რომელიმე ნაწილი გაუარესდება, მაშინ მათი მუშაობის ეფექტურობა გაუარესდება. ეს მდგომარეობა უკავშირდება საკვებში ცოცხალი ატომების არარსებობას ან დეფიციტს, რომლებიც მიეწოდება ქსოვილებსა და უჯრედებს.
რა არის ცოცხალი საკვები? ეს არის საკვები, რომელიც შეიცავს ცოცხალ ორგანულ ფერმენტებს და ატომებს, რომლებიც ნაპოვნი არიან უმი საკვებში.
განვიხილოთ ეს საკითხი ოქსალიუმის მჟავასთან ერთად. საკვებში ოქსილის მჟავა (უმი წვენებში და ბოსტნეულში) არის ორგანული, ის ივსება ფერმენტებით, ანუ ის არა მხოლოდ სასარგებლოა, არამედ სასიცოცხლოა ჩვენი ორგანიზმის ნორმალური ფუნქციონირებისთვის.
მაგრამ თერმულად დამუშავებულ საკვებში ის ხდება არაორგანული და მას აქვს მავნე თვისებები, რომლებიც ზოგჯერ უბრალოდ დამანგრეველი ხდება.
ოქსალიუმის მჟავა ადვილად ურთიერთქმედებს კალციუმთან. თუ ორივე ნივთიერება ორგანულია, მაშინ ოქსალიუმის მჟავა ხელს უწყობს კალციუმის შეწოვას, და ეს ასტიმულირებს სხეულის პერისტალტიკულ ფუნქციებს.
მაგრამ თუ საკვების გადამუშავების დროს ოქსალიუმის მჟავა ხდება არაორგანული, მაშინ იქმნება ნაერთები, რომელშიც კალციუმი განადგურებულია და წარმოიქმნება ოქსალიუმის მჟავების მარილები, ოქსალატები. ეს, თავის მხრივ, იწვევს ძვლოვანი ქსოვილის განადგურებას, ქვების წარმოქმნას, ხელს უწყობს ისეთი დაავადებების წარმოქმნას, როგორიცაა ართრიტი, ართროზი, იმპოტენცია და ა.შ.
აქედან გამომდინარე, უნდა გვახსოვდეს, რომ ოქსილის მჟავას ჭარბი რაოდენობა და მის მიერ წარმოქმნილი ნაერთები შეიძლება ზიანს მიაყენოს სხეულს.
რა თქმა უნდა, თუ საჭმლის მომნელებელი სისტემა ჯანმრთელია, მაშინ ოქსალატები დიდ ზიანს არ მოგაყენებთ, მაგრამ თუ თქვენ დაზარალდებით gout, შარდმჟავას დიათეზი, მაშინ უნდა შეამციროთ პროდუქტების გამოყენება, რომლებიც შეიცავს ოქსილის მჟავას.
საკვებში ოქსილის მჟავას ამაღლებამ შეიძლება გამოიწვიოს მრავალი სხვა სიმპტომი: კუჭქვეშა ჯირკვალი, სისუსტე, ქოშინი, გულისრევა და კრუნჩხვები მუცელში.
ადამიანებისთვის, რომლებიც არ განიცდიან ზემოხსენებულ დაავადებებს, ეს პროდუქტები (ზოგიერთის გამონაკლისის გარდა) არ მოიტანს ზიანს, არამედ მხოლოდ სარგებელს მოუტანს.
ოქსილის მჟავის მოწამვლის სიმპტომები.
დიდი რაოდენობით ოქსალური მჟავის შინაგანი მიღების შემდეგ, ტკივილი ხდება პირის ღრუში, საყლაპავის გასწვრივ და კუჭში. ჩნდება ღებინება, ძაფისებრი პულსი, მოძრაობის გაუარესებული კოორდინაცია. მოგვიანებით - ურემიისა და თირკმლის უკმარისობის ნიშნები.
პირველი დახმარება მჟავის მოწამვლისთვის.
თუ oxalic მჟავა მიიღება პერორალურად, ის უნდა განეიტრალდეს. ამისათვის საჭიროა პაციენტს დანიშნოს კალციუმის მარილები შიდა გამოყენებისთვის (ცარცი, კალციუმის ქლორიდი, კალციუმის გლუკონატი, კალციუმის ლაქტატი და ა.შ.). თუ მდგომარეობა გაუარესდება, პაციენტი საავადმყოფოში გაგზავნეთ.
უსაფრთხოების მოთხოვნები oxalic მჟავის ტრანსპორტირებისა და შენახვისთვის.

გამარჯობა ყველას!
როგორ მოგწონთ ჩემი სტატია ექიმების შესახებ წინა სტატიაში? რას ფიქრობთ ამაზე?
ზოგადად, რატომღაც, ცხოვრება ხშირად მეპირისპირება ამგვარი გაუგებრობით. მახსოვს, როდესაც კურჩატოვიდან უსტ-კამენოგორსკში გადავედი საცხოვრებლად, მე რეგისტრაციისთვის მივედი მოსახლეობის მომსახურების ცენტრში (PSC), სადაც ოპერატორმა დაიწყო ჩემთვის კითხვარის შევსება და განათლება მივიღე. კითხვაზე, ვინ ვარ დიპლომში, ვუპასუხე ”ანალიტიკოს ქიმიკოსს”.
ღარიბი გოგოს ოპერატორს (აშკარად 18 წლის, უკვე აღარ ჰყავდა) კვადრატული თვალები ჰქონდა და თითქმის ჩურჩულით იკითხა ისევ: "ეს ნიშნავს ქიმიის მასწავლებელს, არა?" ბინასთან და რეგისტრაციასთან დაკავშირებული ყველა განსაცდელის შემდეგ, ეს ყველაფერი ჩემთვის ერთნაირი იყო, ასე რომ, მე გავუღიმე: "დიახ, წერე, ქიმიის მასწავლებელი".
ცუდია ცოტა ცნობილი პროფესიის არსებობა
და ამ მოკლე წვეთის შემდეგ, მე ვუბრუნდები ყველაზე საინტერესო ქიმიკატებს, რაზეც ახლახან დავიწყე საუბარი - მჟავებზე. მე უკვე ვისაუბრე ლიმონისა და აცეტილსალიცილის შესახებ.
დღეს ჩვენ ვისაუბრებთ იმაზე, თუ რა არის oxalic მჟავა: გამოყენების ყოველდღიურ ცხოვრებაში, თვისებები და სიფრთხილის ზომები მასთან მუშაობის დროს. ან ფიქრობთ, რომ ეს არ გჭირდებათ, რადგან არსად წააწყდებით? უშედეგოდ. ვნახოთ.
ეს არის ორგანული მჟავა, რომელიც ბუნებაში გვხვდება ზოგიერთ მცენარეში. ყველაზე მეტად მჟავე, ისპანახი და კენჭი. ეს არის ის, ვინც მათ მაწონი გემოს აძლევს. უცნაურია, ბევრია შოკოლადის, ჭარხლისა და ძლიერი შავი ჩაის შემადგენლობაში.
ოქსალიუმის მჟავას მარილებს ეწოდება ოქსალატები. ვფიქრობ, თქვენ ხშირად გსმენიათ ამ სიტყვის შესახებ, განსაკუთრებით მათ, ვისაც პრობლემები აქვს მარილების შეტანაში სახსრებში ან თირკმლის ქვებით - ეს არის ხსნადი კალციუმის ოქსალატები. სწორედ ამიტომ, მკურნალობის დროს, ექიმები გირჩევენ შეამცირონ საკვების გამოყენება, რომელიც შეიცავს უამრავ ოქსილის მჟავას.
ბუნებრივი ოქსილის მჟავების ნაერთები ყველაზე ხშირად კალიუმის ოქსალატებია.
საინტერესოა, რომ ოქსილის მჟავამ მნიშვნელოვანი როლი ითამაშა ორგანული ქიმიის, როგორც მეცნიერების განვითარებაში. ფაქტია, რომ XIX საუკუნის დასაწყისში, მეცნიერებმა ნათლად დაყვეს ყველა ნივთიერება ე.წ მინერალად და ორგანულად. უფრო მეტიც, ყოფილი შეიძლება არსებობდეს მხოლოდ ცოცხალ ორგანიზმებში, ხოლო ეს უკანასკნელნი, შესაბამისად, არაინფიცირებულ ობიექტებში.
და 1824 წელს, გერმანელმა ქიმიკოსმა ფრიდრიხ ვულერმა გაანადგურა ეს იდეები იმით, რომ მან მიიღო ორგანული ნივთიერება (ოქსილის მჟავა) არაორგანული ნივთიერებებისგან. კარგი, ამის შემდეგ, ასეთი აღმოჩენები მიდიოდნენ ერთმანეთის მიყოლებით. შედეგად, მეცნიერებმა მივიდნენ დასკვნამდე, რომ უფსკრული არაორგანულ და ორგანულ ნივთიერებებს შორის არ არსებობს, იგივე კანონები მოქმედებს ყველა მათგანზე.
აქ არის ასეთი საინტერესო ნივთიერება - ეს ოქსალიუმის მჟავა ან „მჟავე”, როგორც ქიმიკოსები უწოდებენ მას ლაბორატორიებში, ხშირად იყენებენ მას ქიმიური ჭურჭლის სარეცხი საშუალებების დასამზადებლად.
ზედმეტია ვთქვა, ეს უზარმაზარია:
ყოველდღიურ ცხოვრებაში მისი ძირითადი გამოყენება სარეცხი საშუალებების ნაწილია, როგორც გაუფერულება და სადეზინფექციო ნივთიერება.
ყველაზე გავრცელებული გამოყენებაა ჟანგის მოცილება. უფრო მეტიც, ოქსალური მჟავის ეს თვისება ადვილია ჟანგით გაჟღენთილი სანტექნიკისთვის, მეტალის ნაწილებისთვის და ტანსაცმელზე ჟანგიანი ლაქებისთვისაც კი.
ერთხელ ჩემმა კოლეგამ ჩამოაგდო თავისი თეთრი სვიტერი, რომ გაეკრა ბატარეა და ვერ შეამჩნია, რომ მასზე ჟანგიანი ლაქები ჰქონდა. შედეგად, ჟანგიანი ლაქები სვიტერზე დარჩა. შემდეგ მე ლაბორატორიაში ვმუშაობდი, მას მივეცით ოქსილის მჟავა, რომლითაც მან შეინახა ტანსაცმელი.
ახლა პრობლემურია სუფთა ოქსალური მჟავის პოვნა და ყიდვა, ყოველ შემთხვევაში, ჩვენს ქვეყანაში, ყაზახეთში, მაგრამ მრავალფეროვან ფხვნილებში შეგიძლიათ იხილოთ მილები, სარეცხი საშუალებები და ასევე „ანტინაკიპინი“. სხვათა შორის, წერის დროს მათ მითხრეს, რომ მისი ნახვა შეგიძლიათ მაღაზიებში მეფუტკრეებისთვის და ვეტერინარული მაღაზიებისთვის.
კარგად, როგორ გამოვიყენოთ იგი? მარტივია. ჩაასხით კოვზი ლიტრი თბილი წყლით - ეს არის გამოსავალი ჟანგის საწინააღმდეგოდ.
უბრალოდ არ დაივიწყოთ სიფრთხილის ზომები! ეს ნივთიერება მიეკუთვნება საფრთხის მეორე კლასს - ის აღიზიანებს ზედა სასუნთქ გზებს, აქვს გამოხატული გამაღიზიანებელი ეფექტი კანზე და ლორწოვან გარსებზე. უფრო მეტიც, ეს ეხება არა მარტო მჟავას, არამედ მის მარილებს. გარდა ამისა, მისი მტვერი აალებადია.
ახლა კი - რამაც გამოიწვია ჩემი დიდი აღშფოთება და შემდეგ - აღშფოთება. როდესაც ამ სტატიისთვის ვეძებდი მასალას, ვხედავდი უამრავ საცნობარო და სპეციალიზებულ ლიტერატურას, როგორც ქაღალდზე, ასევე ელექტრონულ ფორმაში, ასევე ვცდილობდი ინტერნეტში მოძებნოთ ინფორმაცია. მე ვამბობ "მე ვცადე", რადგან თითქმის ყოველ მეორე სტატიაში შევხვდი ასეთ საშინელებას ... არც კი ვიცი რა სიტყვებია ამის აღწერა. განსაჯეთ საკუთარი თავისთვის, აქ მოცემულია სტატიების ნაწილის ეკრანიზაცია ერთ-ერთ ამ საიტზე:
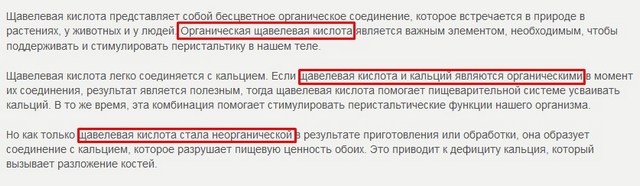
და როგორ მოგწონთ ეს:

როგორ შეიძლება ორგანული ოქსილის მჟავა მოულოდნელად გადაიქცეს არაორგანულად ?! კარგი რა სისულელეა! ნივთიერება ყოველთვის ერთია, თუ მასში რაიმე ქიმიური გარდაქმნა ხდება, მაშინ ის იქცევა სხვა ნივთიერებად, რომელსაც სხვანაირად დაერქმევა, აქვს სხვა სტრუქტურა და სხვა თვისებები.
მაგრამ ისეთი, რომ ნივთიერება მოულოდნელად განიცდის გარკვეულ ქიმიურ გარდაქმნებს და თავისთავად რჩება - ასეთი რამ არ არსებობს! და ორგანული კალციუმი ჭვარტლის სინონიმია! არ არსებობს ორგანული კალციუმი.
განსაკუთრებით კმაყოფილია "კალციუმის განადგურებით", რომელიც ხდება საკვების გადამუშავების დროს. და, იგი, შემთხვევით, არ არის დამუშავებული ბირთვულ რეაქტორში? ყოველივე ამის შემდეგ, მხოლოდ ბირთვულ რეაქციებს შეუძლიათ დაანგრიონ ნებისმიერი ქიმიური ელემენტი.
მოკლედ, თუ ხედავთ მსგავს საიტს - გაიქეცით მთელი ძალით. მათი ავტორები გაუნათლებელი და სულელები არიან. გაუნათლებელი - იმიტომ რომ მათ არ იციან დაწყებითი სკოლის ქიმიის კურსი, მაგრამ სულელები არიან - იმიტომ, რომ ისინი ერთმანეთისაგან კოპირებას ასებენ, თანაც კი არ ფიქრობენ იმაზე, თუ რას წერთ. და არა ვიკიუმი ეს მათ აღარ დაეხმარება.
სტატიაში მოსწონს "ცოცხალი აქტიური გარემო" წყლის შესახებ, რომლის შესახებაც მე უკვე დავწერე.
შესაბამისად, ძალიან დიდი კითხვაა, შესაძლებელია თუ არა ენდოთ ასეთი საიტების რჩევებს. თუ გსურთ - სცადეთ ეს, აარიდეთ ჯანმრთელობა. მე არ ვიქნები
სხვათა შორის, აქ არის საინტერესო ვიდეო, რომელიც ამ საიტებზე არანაკლებ დამანგრევია:
წარმატებებს გისურვებთ ყველას და გქონდეთ კარგი სამუშაო კვირა!
ნატალია ბრაანცევა
- არის უფერო მონოკლინიკური ჰიგიროსკოპული კრისტალები, წყალში ადვილად ხსნადი, შემოიფარგლება ეთილის სპირტით და დიეთილ ეთერით, განზავებულია ქლოროფორმში, ნავთობ ეთერში და ბენზოლში.ქიმიური ფორმულა: C 2 H 2 O 4
 ოქსილის მჟავას გამოყენება.
ოქსილის მჟავას გამოყენება.
- ქიმიურ ინდუსტრიაში (ორგანული სინთეზი, პლასტმასის, მელნის წარმოებაში, საღებავების სინთეზში, პიროტექნიკური კომპოზიციების კომპონენტად);
- ქიმიურ მეტალურგიაში (როგორც კომპოზიციების კომპონენტი ჟანგიდან, მასშტაბისგან, ოქსიდებისგან ლითონების დასუფთავებისთვის); - ანალიზურ ქიმიაში (როგორც იშვიათი დედამიწის ელემენტების ნალექი);
- მიკროსკოპში (როგორც სექციების გაუფერულება);
- ტექსტილისა და ტყავის ინდუსტრიაში (კრეფა ნიჟარა ბეჭდვაში და მატყლისა და აბრეშუმის საღებავი, ტყავის გარუჯვის დროს);
- სინთეზური სარეცხი საშუალებების წარმოებაში (როგორც გაუფერულება და სადეზინფექციო საშუალება, საშარდე ქვის გაწმენდისა და მოცილების საშუალება, სიმკვრივის მარილები და ჟანგი);
- კოსმეტიკურ საშუალებებში (როგორც აქტიური დანამატი კრემებისა და კრემების გასათეთრებელი კრემებისგან);
- წყლის გამწმენდის სისტემებში (წყლის გამტარიანობის გაწმენდისა და შემცირების ქიმიური მეთოდი, გამაგრილებლების გაწმენდა ატომურ ელექტროსადგურებში);
- მედიცინასა და ფარმაცევტებში.
უსაფრთხოების მოთხოვნები.
ოქსალიუმის მჟავა არის აალებადი ნივთიერება; დასახლებულ მდგომარეობაში, ოქსილის მჟავას მტვერი აალებადია; სხეულზე ზემოქმედების ხარისხით, იგი მიეკუთვნება მე -2 საშიშროების კლასის ნივთიერებებს.
მას აქვს ძლიერი გამაღიზიანებელი ეფექტი კანზე, თვალებისა და ზედა სასუნთქი გზების ლორწოვან გარსებზე. ოქსილის მჟავა და მისი მარილები ტოქსიკურია. ოქსალიუმის მჟავასთან მუშაობის დროს უნდა გამოიყენოთ PPE.
შეფუთვა, ტრანსპორტირება და შენახვა.
ტექნიკური oxalic მჟავა შეფუთულია პლასტიკური ჩანთებით ან პლასტიკური ფილმისგან დამზადებული ჩანთებით, ფერადი ბეჭდვით. იგი ასევე შეიძლება შეფუთული იყოს პლაივუდის დასარტყამი ფირის ჩანთის ჩანართით ან რბილი სპეციალიზირებული კონტეინერით ერთჯერადი გამოყენებისთვის.
ოქსალიუმის მჟავა ტრანსპორტირდება ყველა სახის ტრანსპორტით. შეინახეთ მწარმოებლის შეფუთვაში დახურულ, ვენტილაციულ საწყობებში, პლატაზე.
გარანტიის შენახვის ვადა - დამზადების დღიდან 6 თვე.
ოქსალიუმის მჟავა (ეთანედრიუმის მჟავა) - დიბაშური ლიმიტის კარბოქსილის მჟავა.
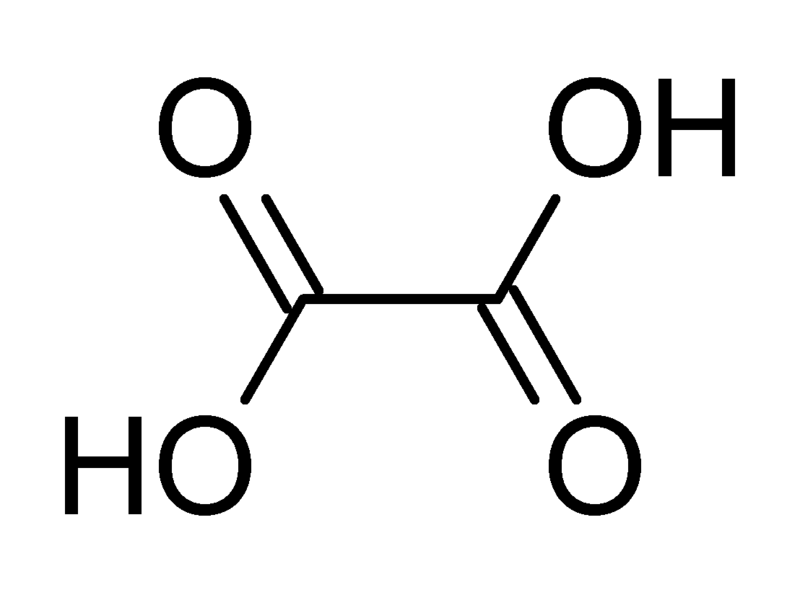
მთლიანი ფორმულა: C 2 H 2 O 4.
სტრუქტურული ფორმულა:
H O O O O H
უფერო მონოკლინიკური ჰიგიროსკოპული კრისტალები, წყალში ადვილად ხსნადი, შემოიფარგლება ეთილის სპირტით და დიეთილ ეთერით, განზავებულია ქლოროფორმში, ნავთობ ეთერში და ბენზოლში. მიეკუთვნება ძლიერ ორგანულ მჟავებს. მას აქვს კარბოქსილის მჟავების დამახასიათებელი ყველა ქიმიური თვისება. ოქსოლიუმის მჟავას მარილებს და ესთერებს ეწოდება ოქსალატები. Oxalic მჟავა ქმნის მჟავე და საშუალო ეთერებს, ამიდებს, მჟავა ქლორიდს. სიმკვრივე 1.36 გ / სმ 3. დნობის წერტილი არის 189.5 ° C, სუბლიმაციის ტემპერატურა 125 ° C, დაშლის ტემპერატურა 100-130 ° C, ხოლო დეკარბოქსილირების ტემპერატურა 166-180 ° C. ცხელი ზედაპირების ან ცეცხლის შეხებისას, ოქსალური მჟავა იშლება, იქმნება მჟავა და ნახშირორჟანგი. ძალზე რეაგირებს ძლიერი დაჟანგვის საშუალებებით, რაც ხანძრისა და აფეთქების საშიშროებას ქმნის. რეაგირებს გარკვეული ვერცხლის ნაერთებით, ასაფეთქებელი ვერცხლის ოქსალატების ფორმირებისთვის.
იშვიათი დედამიწის ლითონების წარმოება არის ის ინდუსტრია, რომელიც მოიხმარს ყველაზე დიდი მოცულობის oxalic მჟავა. სტატისტიკის თანახმად, 1 ტონა ოქსალიუმის მჟავას საჭიროა 1 ტონა იშვიათი დედამიწის ლითონის წარმოება. მეორე უდიდესი მომხმარებელი ფარმაცევტული ინდუსტრიაა. ზემოთ მოყვანილი ორი სექტორის მოხმარების მთლიანი წილი არის ოქსალიუმის მჟავის გლობალური მოხმარების 68%.
გარდა ამისა, ოქსალიუმის მჟავა გამოიყენება საღებავების ინდუსტრიაში (როგორც კატალიზატორი გამძლეობით დაფარვის სამკურნალოდ); წყლის გამწმენდის სისტემებში (წყლის გამტარიანობის გაწმენდისა და შემცირების ქიმიური მეთოდი, ატომური ელექტროსადგურებში გამაგრილებლების გაწმენდა); ქიმიურ მრეწველობაში (ორგანული სინთეზი, პლასტმასის, მელნის წარმოებაში, საღებავების სინთეზში, პიროტექნიკური კომპოზიციების კომპონენტად); ქიმიური მეტალურგიისას (როგორც კომპოზიციების კომპონენტი ჟანგიდან, მასშტაბისგან, ოქსიდებისგან მეტალების დასუფთავებისთვის); ანალიზურ ქიმიაში (როგორც იშვიათი დედამიწის ელემენტების ნალექი); მიკროსკოპში (როგორც სექციების გაუფერულება); სინთეზური სარეცხი საშუალებების წარმოებაში (როგორც გაუფერულება და სადეზინფექციო საშუალება, საშარდე ქვის გაწმენდისა და მოცილების საშუალება, სიმკვრივის მარილები და ჟანგი); ტექსტილისა და ტყავის ინდუსტრიებში (კრეფა ნიჟარა ბეჭდვაში და მატყლისა და აბრეშუმის საღებავი, ტყავის გარუჯვის დროს).

ფოლადის დაწვა ან დაჟანგვა წარმოადგენს ფოლადის ნაწილების ზედაპირზე თხელი წვრილად წვრილი კრისტალური და წვრილად ფოროვანი ოქსიდის ფილმის ფორმირების პროცესს. ფოლადის შერწყმის შედეგად დაიღუპა ორი ფრინველი ერთი ქვით: ნაწილები იძენენ ესთეტიკურ მშვენიერებას და იღებენ სიცოცხლის ხანგრძლივ დაცვას კოროზიისგან.
ოქსალიუმის მჟავა არის ელექტროლიტის ნაწილი ფოლადის წვისთვის. ოქსილის მჟავასთან დამწვრობის მახასიათებელი თვისებაა ოქსიდის ფილმის ლურჯი – შავი ფერი. ელექტროლიტი შედგება მხოლოდ წყლისა და ოქსილის მჟავისაგან. 100 კგ წყალში გამოიყენება 0.3 კგ ოქსალური მჟავა.
ელექტროლიტური ფოლადის დაწვა ხორციელდება ელექტრული დენის გავლენის ქვეშ, 1-1,5 A / dm 2 სიმკვრივით, ძაბვა 6-8 ვ. ვოლტაჟი. ელექტროლიტური ხსნარის ტემპერატურა ოპერაციულ რეჟიმში 25 ° C. დამუშავების დროა 90-100 წუთი. როგორც ანოდი, გამოიყენება ტყვიის ფირფიტა, რომლის ფართობია 1.5-ჯერ მეტი ნაწილის ფართობი. დაჟანგვის შემდეგ, ნაწილი მუშავდება საშრობი 100-110 ° C ტემპერატურაზე.

ალუმინის ანოდიური დაჟანგვა წარმოადგენს მჟავებისა და ტუტეების ხსნარისგან ქიმიურად ან ელექტროქიმიურად ალუმინზე ოქსიდის ფილმის წარმოების პროცესს.
ოქსილის მჟავას ელექტროლიტში ანოდიზაციისას ხდება ფილმების მიღება, რომლებსაც აქვთ კარგი ელექტრული საიზოლაციო თვისებები. ისინი გაუმჭვირვალეა, შეღებილია დეკორატიული ოქროსფერი ტონებით. ამ ელექტროლიტში შეიძლება დამუშავდეს თუჯის ალუმინის შენადნობები, რომლებიც შეიცავს 5% სპილენძს ან 4% სილიკონს. ანოდიზაცია ხორციელდება პირდაპირი ან ალტერნატიული დენზე. DC ანოდიზაცია ხორციელდება 100 კგ წყალში 3-5 კგ ოქსალმჟავას ელექტროლიტში. ოპერაციული რეჟიმი: ელექტროლიტის ტემპერატურა 15-25 ° C, ანოდი დენის სიმკვრივე 1-2 A / dm 2, აბაზანაზე ძაბვა 40-60 V (ელექტროლიზის ბოლოსთვის აღწევს 60-70V). კარგი ელექტრული საიზოლაციო თვისებების მქონე მყარი ფილმების მისაღებად, მათი სისქე უნდა იყოს მინიმუმ 25-40 მიკრონი. მავნე მინარევები, რომლებიც ანოდიზაციის ხარისხს ამცირებს, არის ქლორი და ალუმინი. მათი დასაშვები კონცენტრაცია ელექტროლიტში არის 0,04 გ / ლ და 30 გ / ლ, შესაბამისად.

ხის გაუფერულება, როგორც წესი, ხორციელდება საღებავებამდე ლაქების მოსაშორებლად, მსუბუქია ზედაპირის მოსაპოვებლად. გარდა ამისა, გაუფერულების შემდეგ, ხე უფრო თანაბრად და ლაქების სუფთაა.
ოქსოლიუმის მჟავა (10% ხსნარი) ვრცელდება გაუფერულ ზედაპირზე, მანამდე ნესტიან 20% ნატრიუმის ჰიდროსულფიტის ხსნარით. არაუმეტეს 5 წუთის შემდეგ, გამოყენებული ფორმულირებები გარეცხილია ჩვეულებრივი წყლით.
მსუბუქი სახეობებისთვის - ცაცხვი, არყის, ნეკერჩხალი, სატყუარა - რეკომენდებულია ოქსოლიუმის მჟავას (1.5-6 კგ) ხსნარი ადუღებულ წყალში (100 კგ).
დაჩქარებული გათეთრების მიზნით, შეგიძლიათ გამოიყენოთ შემდეგი შემადგენლობა (კგ): გოგირდმჟავა - 20; oxalic მჟავა - 15; ნატრიუმის პეროქსიდი - 25 (ან წყალბადის ზეჟანგი - 10); წყალი - 1000.

ოქსილის მჟავა ადვილად გამორიცხავს წყალმცენარეებს, მოლუსკებს, მუსკებს, კირს, ჟანგი გემის წყალქვეშა ნაწილიდან, ძრავით, ლილვიდან. ამის გაკეთება, იგი უბრალოდ გამოიყენება და დარჩა გარკვეული ხნით. შემდეგ გარეცხეთ წყლით.
ოქსალიუმის მჟავა ადვილად ხსნის მუდმივ დამაბინძურებლებს, როგორიცაა მტვერი, ოქსიდის ლაქების შავი ლაქები (დურალუმინის კატარღებზე), ჟანგი და ძრავის ზეთი, ცაცხვი გელკატის, პლასტმასის, მეტალისა და ლაქების ზედაპირიდან. ხის გემი oxalic მჟავა იცავს ჩამოსხმისგან.

ეს ეფექტური საშუალებაა ფუტკრების ვარიკოზული დაავადების დროს ფუტკრებში (ფუტკრის დაავადება ვარროლას ტიტით). მკურნალობის შემდეგ ფუტკრები და დედოფლები არ აღინიშნება.
დამუშავება ხდება ერთხელ, სპეციალურად მომზადებული ხსნარით, ფუტკრების მორწყვის მეთოდით, ქუჩაში 5 მლ ხსნარის კურსით.
სამუშაო ხსნარის მომზადება შესაძლებელია ორი გზით ერთი:
1) 100 გ შაქრის, 100 მლ წყალისა და 7.5 გრ ოქსალიუმის მჟავას (GOST 22180-76) შერევით სრულ დაშლამდე. ერთჯერადი მკურნალობის oxaricidal ეფექტურობა მკურნალობის შემდეგ ოთხი დღის განმავლობაში 85%.
2) ოქსალიუმის მჟავა 3.75% კონცენტრაციით, გამოიყენება 20% სიროფში. ფუტკრის კოლონიების დამუშავება ოქსალიუმის მჟავასთან 95% და არ არის დაბალია ბივარის ხარისხთან (92%).
ფუტკრების მორწყვის გზით ოქსალიუმის მჟავას გამოყენების ეკონომიკური ეფექტი, ბივართან მკურნალობისას შედარებით, რომლებსაც აქვთ გამოყენების იგივე მეთოდი, განპირობებულია პრეპარატების ღირებულების განსხვავებით, აგრეთვე იმით, რომ მჟავასთან მკურნალობა ტარდება ერთხელ, ორჯერ კი ბივართან. ოქსალიუმის მჟავასთან ერთჯერადი მკურნალობის ჯამური ღირებულება ბივართან ორმაგ მკურნალობაზე ნაკლებია, ვიდრე გაორმაგებული (შრომის ხარჯების, შაქრის და მჟავის გათვალისწინებით).
ოქსილის მჟავა ვარიკოზის წინააღმდეგ ბრძოლის უაღრესად ეფექტური ეკოლოგიური მეთოდია. აკარიციდული ეფექტურობის თვალსაზრისით, იგი არ არის inferior ამ პერიოდისთვის რეკომენდებული ბიპინით და ბივრით. ამ მეთოდით ოქსალიუმის მჟავასთან მკურნალობა უარყოფითად არ მოქმედებს ფუტკრის კოლონიებზე. ოქსალიუმის მჟავის გამოყენებამ შეიძლება გააუმჯობესოს შედეგად მიღებული პროდუქტების სანიტარული ხარისხი.
![]()
Oxalic მჟავა ასუფთავებს ლითონებს და ზოლები რკინის, თუთიის, სპილენძის ჭაბურღილისგან. იგი ინარჩუნებს საღებავს და ლითონს. ოქსალიუმის მჟავას იყენებენ მუზეუმის მუშები და არქეოლოგები მონეტების, ბალთების, მუზარადების, კარტრიჯების, კერძების დასუფთავების მიზნით და მრავალი სხვა.
დასუფთავებისთვის, გამოიყენება ოქსალიუმის მჟავას 5% -იანი ხსნარი (50 გრამი 1 ლიტრზე). ნივთის მდგომარეობიდან გამომდინარე - ოქსალიუმის მჟავასთან გაწმენდა გრძელდება 20-40 წუთის განმავლობაში თბილ ხსნარში, ხოლო 3 დღის განმავლობაში ცივ ხსნარში. ყველაზე ხშირად ისინი იყენებენ პლასტმასის კონტეინერს გათბობით წყლის აბაზანაში. დახარჯული ოქსილის მჟავას ხსნარის რეაქციის უნარი დროთა განმავლობაში ასუსტებს. ეს დამოკიდებულია ხსნარით ამოღებული ოქსიდების რაოდენობაზე.

წყლის სიმტკიცე დამოკიდებულია კალციუმის და მაგნიუმის მარილების რაოდენობაზე. ოქსალიუმის მჟავა რეაგირებს ამ მარილებზე. ამ რეაქციის პროდუქტები ადიდებს.
დარბილებული წყალი არ აალაგებს ნიადაგს და ზრდის ხილისა და ბოსტნეულის მოსავალს, აუმჯობესებს შიდა მცენარეების განვითარებას.
წყლის დარბილების მიზნით, გამოიყენება ოქსილის მჟავას 1% -იანი ხსნარი (10 გრამი 1 ლიტრზე). ოთახის ტემპერატურაზე, წყალი საკმარისია დღეში. ვიზუალურად, წყალი გამჭვირვალე გახდება. შემდეგ ნალექი გამოყოფილია. ამისათვის, ფრთხილად სანიაღვრე წყალი. მარილებით მარილი არ არის საშიში, მაგრამ არ ექვემდებარება შემდგომი გამოყენებას ფერმაში.
Oxalic მჟავა ძლიერი მჟავაა, რომელიც მყარი ფორმით ან კონცენტრირებულ ხსნარებში შეიძლება გამოიწვიოს კანის, თვალების ან ლორწოვანი გარსების დამწვრობა. ოქსილის მჟავას დაბალი კონცენტრაციებიც კი (5-დან 10% -მდე) გახანგრძლივებული ზემოქმედებით არის გამღიზიანებლები. დაფიქსირებულია მხოლოდ 5 გ ოქსმჟავას გადაყლაპვის შემდეგ დაღუპულთა შემთხვევები. მოწამვლის სიმპტომები სწრაფად ჩნდება: შოკი, კოლაფსი, კრუნჩხვები. ასეთ შემთხვევებში თირკმელების დაზიანება აღინიშნება თირკმლის არხებში კალციუმის ოქსილატის ნალექით. კონვულსიები შეიძლება გამოწვეული იყოს ჰიპოკალციემიით. ოქსილის მჟავას ან ოქსალიუმის კალიუმის ხსნარებით კანის გახანგრძლივება იწვევს ადგილობრივ ტკივილს, თითების ციანოზი და განგრევულ ცვლილებებს. ცხადია, ეს განპირობებულია ოქსილის მჟავის ადგილობრივი შეწოვით, რასაც იწვევს ართრიტი. ქრონიკული სისტემური დაავადებები ოქსილის მჟავას მტვრის ინჰალაციისგან ძალზე იშვიათია, თუმცა ლიტერატურაში აღწერილია შემთხვევა, როდესაც ცხელ ოქსილის მჟავას ორთქლზე მყოფ პირს (სავარაუდოდ, შეიცავს ოქსილის მჟავას აეროზოლს), აქვს სიმპტომები, როგორიცაა წონის დაკლება და ზედა სასუნთქი გზების ქრონიკული ანთება. . ოქსალიუმის მჟავას მტვრის ძლიერი მჟავის ეფექტის გამო, სამრეწველო შენობების ჰაერში მისი შემცველობა ფრთხილად უნდა იქნას მონიტორინგი და არ უნდა აღემატებოდეს კონცენტრაციებს, რაც უსაფრთხოა ჯანმრთელობისთვის.
ინდუსტრიაში, ოქსილის მჟავა მიიღება ნახშირწყლების, ალკოჰოლების და გლიკოლების დაჟანგვით HNO 3 და H 2 SO 4 ნაზავით V2 O 5 თანდასწრებით, ან ეთილენისა და აცეტილენის HNO 3 თანდათანობით დაჟანგვით PdCl 2 ან Pd (NO 3) 2 და ასევე პროპილენის დაჟანგვით თხევადი 22.
განათლების ფედერალური სააგენტო
უმაღლესი პროფესიული განათლების სახელმწიფო სასწავლო დაწესებულება
ვოლგოგრადის სახელმწიფო ტექნიკური უნივერსიტეტი
(VolgSTU)
განყოფილება "მაღალი მოლეკულური წონის და ბოჭკოვანი მასალების ტექნოლოგია"
სემესტრის მუშაობა
დისციპლინა "ქიმიური პროცესების საფუძვლები"
თემა: ”პროცესების დახასიათება, რომლებიც ხვდება ოქსილის მჟავის სინთეზში. მასალისა და სითბოს ბალანსის გაანგარიშება. ”
ვოლგოგრადი 2011
ქიმიური თვისებები.
ფიზიკური თვისებები.
მოპოვების მეთოდები.
განაცხადი
გაყიდვების ბაზარი
GOST გასაყიდად
მატერიალური ბალანსი
სითბოს ბალანსი
ქიმიური თვისებები:
ოქსალიუმის მჟავა (ეთანდირიუმის მჟავა) C 2 H 2 O 4 არის დიბაზური გაჯერებული კარბოქსილის მჟავა. მიეკუთვნება ძლიერ ორგანულ მჟავებს. მას აქვს კარბოქსილის მჟავების დამახასიათებელი ყველა ქიმიური თვისება. ოქსოლიუმის მჟავას მარილებს და ესთერებს ეწოდება ოქსალატები. იგი ბუნებაში გვხვდება მჟავე და ზოგიერთ სხვა მცენარეში კალიუმის და კალციუმის ოქსალატების სახით.
ოქსალიუმის მჟავა პირველად სინთეზირდა 1842 წელს გერმანელმა ქიმიკოსმა ფრიდრიხ ვულერმა ტიზიანისგან. ოქსალიუმის მჟავა (ან ოქსალატის იონი C 2 O 4 2-) არის შემცირების აგენტი (discolors KMnO4 გადაწყვეტა).
Oxalic მჟავა ადვილად ხსნადი წყალში და ალკოჰოლში. ეს არის შედარებით ძლიერი ორგანული მჟავა (საშიშროების კლასი 3), NOOS-COOH, არის უფერო ჰიგიროსკოპიული კრისტალები, ადვილად ხსნადი წყალში, შეზღუდულია ეთილ ალკოჰოლსა და დიეთილ ეთერში, უხსნადი ქლოროფორმში, ნავთობის ეთერში და ბენზოლში. ქმნის კომპოზიციის დიჰიდრატს C 2 H 2 O 4 * 2H 2 O. აალებადი ნივთიერება, დასახლებულ მდგომარეობაში, ხანძრის საშიშროება. მას აქვს ძლიერი გამაღიზიანებელი ეფექტი კანზე, თვალებისა და ზედა სასუნთქი გზების ლორწოვან გარსებზე.
ოქსლის მჟავას აქვს კარბოქსილის მჟავების დამახასიათებელი ქიმიური თვისებები, წარმოქმნის წარმოებულების ორი მწკრივი. ოქსოლიუმის მჟავას მარილებს და ესთერებს ეწოდება ოქსალატები. Oxalic მჟავა ქმნის მჟავე და საშუალო ეთერებს, ამიდებს, მჟავა ქლორიდს.
Oxalic მჟავა გვხვდება sorrel და rhubarb, როგორც კალიუმის oxalate.
ეს მჟავა მცენარეების სამყაროში ძალზე გავრცელებულია - მარილების სახით ის გვხვდება მჟავე, მჟავას, კენკრის ფოთლებში და ა.შ. ამ მჟავას მარილებს და ეთერებს აქვთ ტრივიალური სახელი - ოქსალატები (ბერძნულიდან. "ოქსალისი" - მჟავე).
ასევე გამოირჩევა მჟავების ზოგადი თვისებები. რადგან მას აქვს ფუნქციური კარბოქსილის ჯგუფი. მარილის წარმოქმნის რეაქცია ამტკიცებს მჟავე თვისებებს ფორმული მჟავას. ამ შემთხვევაში, მარილები იქმნება - აყალიბებს.
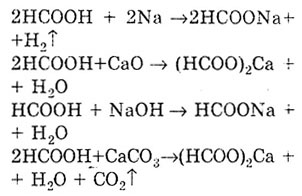
ყველა კარბოქსილის მჟავების მსგავსად, formic მჟავა ქმნის ესთერებს.
ეთერიფიკაციის რეაქცია:
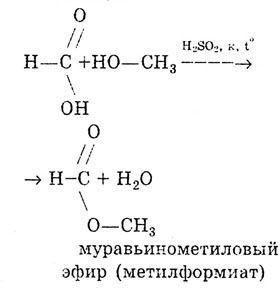
ფორმული მჟავა სხვა კარბოქსილის მჟავებისგან განსხვავდება იმით, რომ მასში არსებული კარბოქსილის ჯგუფი არ არის შემოსაზღვრული ნახშირწყალბადების რადიკალთან, არამედ წყალბადის ატომთან. ამიტომ, ფორმინის მჟავა შეიძლება ჩაითვალოს როგორც მჟავა და როგორც ალდეჰიდი:
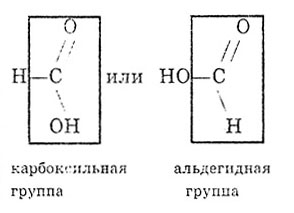
ალდეჰიდების მსგავსად, ფორმინის მჟავას შეუძლია ჟანგავს:
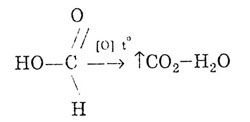
ფორმული მჟავა იძლევა "ვერცხლის სარკის" რეაქციას:
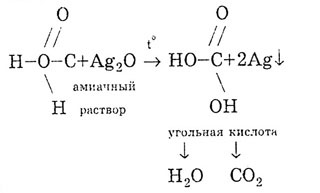
ფორმალური მჟავა იშლება გათბობაზე:
![]()
formic მჟავა მიეკუთვნება მონობაზური კარბოქსილის მჟავების ჰომოლოგიურ სერიას
ფიზიკური თვისებები:
სუბლიმაციის ტემპერატურა: იხ. შენიშვნები ° C
დნობის წერტილი: 102 ° C
ფარდობითი სიმჭიდროვე (წყალი \u003d 1): 1.7
წყალში ხსნადობა, გ / 100 მლ: 10
ორთქლის წნევა, Pa ტემპერატურა 30 ° C- ზე: იხ. შენიშვნები
ფარდობის სიმკვრივე (ჰაერი \u003d 1): 3.1
ოქსალიუმის მჟავა ერთ-ერთი ყველაზე ძლიერი კარბოქსილის მჟავაა, გაცილებით უპირატესობა აქვს მის ჰომოლოგებს.
ეთანდიუმის მჟავა გამოირჩევა შემცირების თვისებებით: კალიუმის პერმანგანატის მჟავას ხსნარში, იგი ჟანგბადიდან ნახშირორჟანგიდან (IV) და წყალში ჟანგდება.
გოგირდის მჟავის თანდასწრებით თბება, ხდება დეკარბოქსილირება და მიიღება ნახშირორჟანგი (IV) და ფორმული მჟავა.
ნორმალური სტრუქტურის ცხიმოვანი მჟავების დუღილის წერტილები ბუნებრივად იზრდება, როდესაც ნახშირბადის ატომების რაოდენობა იზრდება. დადგინდა, რომ მჟავების მოლეკულები დაკავშირებულია ისე, რომ წყალი ან ალკოჰოლის მოლეკულები უკავშირდება. ქვედა მჟავები კარგად არის გამოხდილი წყლის ორთქლით, რის გამოც მათ ჩვეულებრივ უწოდებენ არასტაბილურ ცხიმოვან მჟავებს.
ზოგადად მატულობს მონობაზური მჟავების დნობის წერტილები, რომელთა მოლეკულებში ნახშირბადის ატომების რიცხვი მატდება. მაგრამ ამავე დროს, შეინიშნება შემდეგი რეგულარულობა: მჟავები, რომლებსაც აქვთ ჩვეულებრივი ჯაჭვი, რომელსაც ნახშირბადის ატომებიც კი აქვთ, ჩვეულებრივ დნება უფრო მაღალ ტემპერატურაზე, ვიდრე ჰომოლოგური სერიის წინა და შემდგომ წევრები, რომელთაც უცნაური აქვთ ნახშირბადის ატომები.
ქიმიური საფრთხეები:
ნივთიერება იშლება სწრაფად, დაახლოებით 150 ° C ზემოთ, ტოქსიკური გაზის წარმოქმნით. წყალხსნარი არის საშუალო სიძლიერის მჟავა, რომელიც ძალზე რეაგირებს ძლიერი ბაზებით. ძალზე რეაგირებს ჟანგვითი აგენტებით, რის შედეგადაც ხანძარი და აფეთქება იწვევს. რეაგირებს ვერცხლით, ასაფეთქებელი პროდუქტების წარმოებისთვის.
განაცხადი.
ოქსალიუმის მჟავა და მისი მარილები გამოიყენება ტექსტილისა და ტყავის ინდუსტრიაში, როგორც ურდოს; ანოდური აბაზანების კომპონენტის სახით Al, Ti და Sn საიზოლაციო მასალის შესანახად; როგორც რეაგენტი ანალიტიკურ და ორგანულ ქიმიაში; კომპოზიციების კომპონენტი ჟანგიდან და ოქსიდებიდან ლითონების დასუფთავებისთვის; იშვიათი დედამიწის დეპონირებისთვის. ოქსიამიდი არის ცელულოზის ნიტრატების სტაბილიზატორი, ციანი არის რეაგენტი ორგანულ სინთეზში, ოქსალილის ქლორიდი წარმოადგენს ქლორირების, ქლოროკარბონილირების და ურთიერთკავშირის საწინააღმდეგო რეაგენტს ორგანულ სინთეზში. დიალკილ ოქსალატები, ძირითადად დიეთილ ოქსალატი და დიბუტილ ოქსილატი, გამოიყენება ცელულოზის გამხსნელებად; ოქსილის მჟავისა და შემცვლელი ფენოლების ზოგიერთი ესტერი - როგორც ქიმიოუმენესცენტური რეაქტივები.
ოქსალიუმის მჟავა გამოიყენება ლითონების გასაპრიალებლად, ხე-ტყის წარმოებაში, ურანის გასაწმენდად
ოქსალიუმის მჟავისა და მისი მარილების (ოქსალატები) გამოყენების სფეროები:
ქიმიურ მრეწველობაში (ორგანული სინთეზი, პლასტმასის, მელნის წარმოებაში, საღებავების სინთეზში, პიროტექნიკური კომპოზიციების კომპონენტად);
ქიმიური მეტალურგიისას (როგორც კომპოზიციების კომპონენტი ჟანგიდან, მასშტაბისგან, ოქსიდებისგან მეტალების დასუფთავებისთვის);
ანალიზურ ქიმიაში (როგორც იშვიათი დედამიწის ელემენტების ნალექი);
მიკროსკოპში (როგორც სექციების გაუფერულება);
ტექსტილისა და ტყავის ინდუსტრიებში (კრეფა ნიჟარა ბეჭდვაში და მატყლისა და აბრეშუმის საღებავი, ტყავის გარუჯვის დროს);
სინთეზური სარეცხი საშუალებების წარმოებაში (როგორც გაუფერულება და სადეზინფექციო საშუალება, საშარდე ქვის გაწმენდისა და მოცილების საშუალება, სიმკვრივის მარილები და ჟანგი);
კოსმეტიკაში (როგორც აქტიური დანამატი, კრემების და კრემების გასათეთრებელი კრემებისგან);
წყლის გამწმენდის სისტემებში (წყლის გამტარიანობის გაწმენდისა და შემცირების ქიმიური მეთოდი, ატომური ელექტროსადგურებში გამაგრილებლების გაწმენდა);
მედიცინასა და ფარმაცევტებში.
მოპოვების მეთოდები:
1) როგორც ქვეპროდუქტი ბეტანის თხევადი ფაზის დაჟანგვით ძმარმჟავას წარმოებაში.
2) მეთანოლის დაჟანგვა:
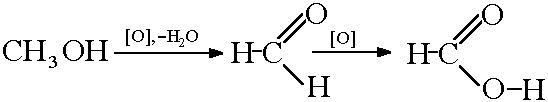
ნახშირბადის მონოქსიდის რეაქცია ნატრიუმის ჰიდროქსიდთან:
NaOH + CO → HCOONa (+ H3SO4, −Na2SO4) HCOOH
ეს არის მთავარი ინდუსტრიული მეთოდი, რომელიც ხორციელდება ორ ეტაპზე: პირველ ეტაპზე, ნახშირორჟანგი 0.6-0.8 მპა-ზე ზეწოლის ქვეშ, გადის ნატრიუმის ჰიდროქსიდში გაცხელებული ტემპერატურა 120-130 ° C- მდე; მეორე ეტაპზე, ნატრიუმის ფორმატს მკურნალობენ გოგირდმჟავას და პროდუქტი ვაკუუმურია დისტილირებული.
გლიცეროლის მჟავების გლიცეროლის ეთერების დაშლა. ამის გაკეთება, უწყლო გლიცერინი ერთად oxalic მჟავა თბება, ხოლო წყალი გამოხდილი off და იქმნება oxalic esters. შემდგომი გათბობით, ეთერები იშლება, იხსნება ნახშირორჟანგი და იქმნება ფორმალური ესტერიები, რომლებიც წყალთან ერთად დაშლის შემდეგ წარმოქმნიან მჟავას და გლიცერინს.
| დაკავშირებული სტატიები: | |
|
ინტერიერი, დეკორი, საცავი, სახლის იდეა, სკანდინავიური სტილი, კალათაში, ნაქსოვი კალათის, ჟანგისფერი, გააკეთე საკუთარი თავისთვის diy, ხელნაკეთი, ინტერიერი, დეკორი, ნაქსოვი, ქსოვის ყუთი
სულ მალე, ზაფხული დადგება და ჩვენთან ერთად გააზიარებს ყველაფერს, რაც მას აქვს: ... ოქსილის მჟავა: რა ვიცით ამის შესახებ
გამარჯობა ყველას! ბევრმა იცის, რომ ოქსილის მჟავა იწვევს ... რა არის სტარტაპი და ვინ არიან სტარტაპები - როგორ შევქმნათ მინიმალური ინვესტიციით და ყველაზე წარმატებული მაგალითები
თარგმანი ეს სახელმძღვანელო კლასიკური შეტყობინებების სერიაა, რომლებიც განიხილება ... | |