Čitateľská voľba
Populárne články
Ahoj všetci! Mnoho ľudí vie, že kyselina šťaveľová spôsobuje tvorbu obličkových kameňov. Ale o tom, čo je to za látku a kde je obsiahnutá a ako sa používa, to veľa ľudí nevie. Z tohto kognitívneho hľadiska je tento článok o tomto.
Nemecký chemik Friedrich Wöhler v roku 1824 najprv syntetizoval kyselinu šťaveľovú. Kyselina šťaveľová (vedecký názov je kyselina etándiová) patrí do skupiny organických kyselín. Kyselina šťaveľová sa v prírode nachádza vo voľnom stave a vo forme šťaveľanov vápenatých a draselných.
Trochu o chemických a fyzikálnych vlastnostiach kyseliny šťaveľovej.
Kyselina šťaveľová je kryštalická, hygroskopická bezfarebná látka bez zápachu. Je čiastočne rozpustný v alkohole (etanol), vode. Vytvára dihydrát kyseliny šťaveľovej.
Kyselina šťaveľová
Získanie kyseliny šťaveľovej:
Vieme, že fyzická kondícia človeka do značnej miery závisí od správneho fungovania svalov a nervov. Fungovanie obehového systému, tráviaceho traktu a vylučovacích orgánov je založené na peristaltických pohyboch, ktoré sú vlnovitej povahy a pozostávajú z postupnej relaxácie a sťahovania svalov a nervov, ktorých účinnosť závisí od ich fyzického stavu.
Kyselina šťaveľová je dobrým stimulátorom funkcie svalov a nervov.
Malo by sa pamätať na to, že životne dôležité procesy v našom tele budú aktívne a živé, ak budú tkanivá a bunky v orgánoch mladé a zdravé. Ak sa niektoré časti našich orgánov začnú zhoršovať, účinnosť ich práce sa začne zhoršovať. Tento stav je spojený s neprítomnosťou alebo nedostatkom živých atómov v potrave, ktoré sa dodávajú do tkanív a buniek.
Čo je to živé jedlo? Je to potravina, ktorá obsahuje živé organické enzýmy a atómy nachádzajúce sa v surových potravinách.
Zoberme si tento problém s kyselinou šťaveľovou ako príklad. Kyselina šťaveľová v potravinách (v surových šťavách a zelenine) je organická, je plná enzýmov, to znamená, že je nielen užitočná, ale aj životne dôležitá pre normálne fungovanie nášho tela.
V tepelne spracovaných potravinách sa však stáva anorganickou a má škodlivé vlastnosti, ktoré sa niekedy jednoducho ničia.
Kyselina šťaveľová ľahko reaguje s vápnikom. Ak sú obe organické látky, potom kyselina šťaveľová podporuje vstrebávanie vápnika, čo stimuluje peristaltické funkcie organizmu.
Ak sa však kyselina šťaveľová počas spracovania potravín stane anorganickou, potom sa vytvoria zlúčeniny, v ktorých sa rozloží vápnik a vytvoria sa soli kyseliny šťaveľovej, oxaláty. To zasa spôsobuje deštrukciu kostného tkaniva, tvorbu kameňov, prispieva k výskytu chorôb, ako sú artritída, artróza, impotencia atď.
Preto by sa malo pamätať na to, že nadbytok kyseliny šťaveľovej a z nej vznikajúcich zlúčenín môže poškodiť telo.
Samozrejme, ak je tráviaci systém zdravý, potom oxaláty nespôsobia veľa škôd, ale ak trpíte dnou, diatézou kyseliny močovej, mali by ste znížiť používanie výrobkov obsahujúcich kyselinu šťaveľovú.
Zvýšená kyselina šťaveľová v potravinách môže spôsobiť celý rad ďalších príznakov: poruchy trávenia, slabosť, dýchavičnosť, nevoľnosť a kŕče v žalúdku.
Pre ľudí, ktorí netrpia vyššie uvedenými chorobami, tieto výrobky (s výnimkou niektorých) neprinesú škodu, ale len úžitok.
Príznaky otravy kyselinou šťaveľovou.
Po vnútornom príjme veľkého množstva kyseliny šťaveľovej sa vyskytuje bolesť v ústnej dutine, pozdĺž pažeráka a žalúdka. Objavujú sa zvracanie, vláknitý pulz, zhoršená koordinácia pohybu. Neskôr - príznaky urémie a zlyhania obličiek.
Prvá pomoc pri otrave kyselinou.
Ak sa kyselina šťaveľová užíva perorálne, musí sa neutralizovať. Preto musí byť pacientovi predpísané vápenaté soli na vnútorné použitie (krieda, chlorid vápenatý, glukonát vápenatý, laktát vápenatý atď.). Ak sa stav zhorší, pošlite pacienta do nemocnice.
Bezpečnostné požiadavky na prepravu a skladovanie kyseliny šťaveľovej.

Ahoj všetci!
Ako sa vám páči môj príbeh o lekároch v predchádzajúcom článku? Čo si o tom myslíš?
Vo všeobecnosti mi život z nejakého dôvodu často čelí takému nedorozumeniu. Pamätám si, že keď som sa presťahoval z Kurchatova do Ust-Kamenogorska, išiel som sa zaregistrovať do Populačného servisného centra (PSC), kde mi operátor začal vyplňovať dotazník a dostával sa na vzdelanie. Na otázku, kto som v diplome, som odpovedal „analytickému chemikovi“.
Chudobná dievča, kameramanka (očividne už viac ako 18 rokov), mala štvorcové oči a takmer šepka sa znova opýtala: „Znamená to učiteľ chémie, však?“ Po všetkých utrpeniach v byte a registrácii to pre mňa bolo rovnaké, tak som prikývol: „Áno, píšte, učiteľ chémie.“
Je zlé mať málo známe povolanie 🙂
A po tejto krátkej digresii sa vraciam k najzaujímavejším chemikáliám, o ktorých som nedávno začal hovoriť - kyselinám. Už som hovoril o citróne a acetylsalicyle.
Dnes budeme hovoriť o tom, čo je kyselina šťaveľová: o použití v každodennom živote, o vlastnostiach a bezpečnostných opatreniach pri práci s ňou. Alebo si myslíte, že to nepotrebujete, pretože sa s ním nikde nestretnete? Nadarmo. Pozrime sa.
Je to organická kyselina, ktorá sa v niektorých rastlinách vyskytuje v prírode. Najviac zo všetkých v šťave, špenáte a rebarbore. Je to ona, ktorá im dáva kyslú chuť. Napodiv je toho veľa v čokoláde, repe a silnom čiernom čaji.
Soli kyseliny šťaveľovej sa nazývajú oxaláty. Myslím, že ste toto slovo často počuli, najmä tí, ktorí majú problémy s ukladaním solí v kĺboch \u200b\u200balebo s obličkovými kameňmi - sú to nerozpustné šťaveľany vápenaté. Preto lekári počas liečby odporúčajú obmedziť používanie potravín, ktoré obsahujú veľa kyseliny šťaveľovej.
Prírodné zlúčeniny kyseliny šťaveľovej sú najčastejšie oxaláty draslíka.
Zaujímavé je, že kyselina šťaveľová zohrávala významnú úlohu vo vývoji organickej chémie ako vedy. Faktom je, že na začiatku 19. storočia vedci jasne rozdelili všetky látky na tzv. Minerálne a organické látky. Okrem toho by prvý mohol existovať iba v živých organizmoch a druhý v neživých predmetoch.
A v roku 1824 nemecký chemik Friedrich Wöhler zničil tieto myšlienky tým, že dostal organickú hmotu (kyselinu šťaveľovú) z anorganických látok. Potom tieto objavy išli jeden po druhom. V dôsledku toho vedci dospeli k záveru, že priepasť medzi anorganickými a organickými látkami neexistuje, na všetky sa vzťahujú rovnaké zákony.
Tu je taká zaujímavá látka - táto kyselina šťaveľová alebo „šťaveľ“, ako ju chemici nazývajú v laboratóriách a často ju používajú na prípravu zmesí na umývanie chemických jedál.
Netreba dodávať, že je obrovský:
V každodennom živote je jeho hlavná aplikácia súčasťou detergentov ako bieliaca a dezinfekčná látka.
Najbežnejším použitím je odstránenie hrdze. Okrem toho je táto vlastnosť kyseliny šťaveľovej ľahko popraskateľná s hrdzou skutočne pre vodoinštalatérstvo a pre kovové časti a dokonca aj pre škvrny odiev na odevoch.
Raz jeden môj kolega zavesil svoj biely sveter, aby uschol na batérii, a nevšimol si, že na ňom boli pruhy hrdze. V dôsledku toho na sveter zostali hrdzavé škvrny. Potom som pracoval v laboratóriu, dali sme mu nejakú kyselinu šťaveľovú, s ktorou si uložil šaty.
Teraz je problematické nájsť a kúpiť čistú kyselinu šťaveľovú, prinajmenšom v našej krajine, v Kazachstane, ale dá sa ľahko nájsť v širokej škále práškov na čistenie potrubí, čistiacich prostriedkov a tiež „antinakipínu“. Mimochodom, pri písaní mi povedali, že sa dá nájsť v obchodoch pre včelárov a vo veterinárnych obchodoch.
Ako to používať? Ľahko. Čajovú lyžičku rozpustite v litri teplej vody - to je riešenie proti hrdzi.
Nezabudnite na bezpečnostné opatrenia! Táto látka patrí do druhej triedy nebezpečenstva - dráždi horné dýchacie cesty, má výrazný dráždivý účinok na pokožku a sliznice. Okrem toho sa to týka nielen samotnej kyseliny, ale aj jej solí. Okrem toho je prach horľavý.
A teraz - čo spôsobilo moje veľké zmätenie, a potom - pobúrenie. Keď som hľadal materiál pre tento článok, prezrel som si veľa referenčnej a odbornej literatúry v papierovej aj elektronickej podobe a tiež som sa snažil hľadať informácie na internete. Hovorím „Skúsil som“, pretože takmer v každom druhom článku som narazil na takú hrôzu ... Neviem ani, aké slová to popisujú. Posúďte sami, tu je snímka obrazovky časti článku na jednom z týchto serverov:
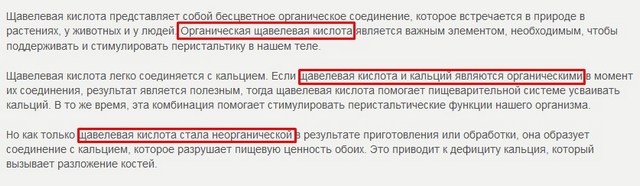
A ako sa vám to páči:

Ako sa môže organická kyselina šťaveľová náhle zmeniť na anorganickú? Aký nezmysel! Látka je vždy jedna, ak s ňou dôjde k nejakej chemickej premene, potom sa zmení na inú látku, ktorá sa bude nazývať inak, bude mať inú štruktúru a ďalšie vlastnosti.
Ale tak, že látka náhle prechádza nejakými chemickými transformáciami a zostáva sama osebe - taká vec neexistuje! A organický vápnik je synonymom sadze! Neexistuje žiadny organický vápnik.
Obzvlášť potešený je „rozklad vápnika“, ku ktorému dochádza pri spracovaní potravín. A náhodou nie je spracovaná v jadrovom reaktore? Koniec koncov, iba jadrové reakcie sú schopné zničiť akýkoľvek chemický prvok.
Stručne povedané, ak vidíte podobné stránky - spustite z nich všetku svoju moc. Ich autori sú negramotní a hlúpi. Negramotní - pretože nepoznajú kurz chémie základnej školy, ale sú hlúpi, pretože tieto nezmysly kopírujú jeden od druhého bez toho, aby premýšľali o tom, čo píšu. A nie vikium už im to nepomôže.
Je to ako v článku o vode s „živým aktívnym prostredím“, o ktorom som už písal.
Preto veľmi veľkou otázkou je, či je možné dôverovať radám z takýchto stránok. Ak chcete - vyskúšajte to, riskujte svoje zdravie. A ja nebudem.
Mimochodom, tu je zaujímavé video, ktoré ma zasiahlo nie menej ako tieto stránky:
Veľa šťastia všetkým a dobrý pracovný týždeň!
Natalya Bryantseva
- sú bezfarebné monoklinické hygroskopické kryštály, ľahko rozpustné vo vode, obmedzené na etylalkohol a dietyléter, nerozpustné v chloroforme, petroléteri a benzéne.Chemický vzorec: C2H204
 Použitie kyseliny šťaveľovej.
Použitie kyseliny šťaveľovej.
- v chemickom priemysle (organická syntéza, výroba plastov, tlačiarenských farieb, syntéza farbív ako súčasť pyrotechnických kompozícií);
- v chemickej metalurgii (ako súčasť zmesí na čistenie kovov od hrdze, vodného kameňa, oxidov), - v analytickej chémii (ako zrazenina prvkov vzácnych zemín);
- v mikroskopii (ako bielidlo rezov);
- v textilnom a kožiarskom priemysle (morenie sieťotlačou a farbenie vlny a hodvábu, pri činení koží);
- pri výrobe syntetických detergentov (ako bieliace a dezinfekčné prostriedky, prostriedky na čistenie a odstraňovanie močového kameňa, tvrdých solí a hrdze);
- v kozmetike (ako aktívna prísada pri bielení krémov a krémov z pihy);
- v systémoch čistenia vody (chemická metóda čistenia a znižovania tvrdosti vody, čistenie chladív v jadrových elektrárňach);
- v medicíne a farmaceutických výrobkoch.
Bezpečnostné požiadavky.
Kyselina šťaveľová je horľavá látka, v usadenom stave je prach kyseliny šťaveľovej horľavý, podľa stupňa vystavenia organizmu patrí medzi látky 2. triedy nebezpečnosti.
Má silný dráždivý účinok na pokožku, sliznice očí a horné dýchacie cesty. Kyselina šťavelová a jej soli sú jedovaté. Pri práci s kyselinou šťaveľovou by sa mal používať OOP.
Balenie, preprava a skladovanie.
Technická kyselina šťaveľová sa balí do plastových vreciek alebo do vreciek z plastovej fólie s farebnou potlačou. Môže byť tiež balený do preglejkových sudov s vložkou z fóliového vrecka alebo mäkkých špecializovaných nádob na jedno použitie.
Kyselina šťaveľová sa prepravuje všetkými spôsobmi dopravy. Skladujte v baleniach výrobcu v uzavretých, vetraných skladoch na paletách.
Záručná doba skladovania - 6 mesiacov od dátumu výroby.
Kyselina šťaveľová (kyselina etándiová) - dibázická limitná karboxylová kyselina.
Hrubý vzorec: C2H204.
Štrukturálny vzorec:
H O O O H H
Bezfarebné monoklinické hygroskopické kryštály, ľahko rozpustné vo vode, obmedzené na etylalkohol a dietyléter, nerozpustné v chloroforme, petroléteri a benzéne. Patrí medzi silné organické kyseliny. Má všetky chemické vlastnosti charakteristické pre karboxylové kyseliny. Soli a estery kyseliny šťaveľovej sa nazývajú oxaláty. Kyselina šťaveľová tvorí kyslé a stredné estery, amidy, chlorid kyseliny. Hustota 1,36 g / cm3. Teplota topenia je 189,5 ° C, teplota sublimácie je 125 ° C, teplota rozkladu je 100 - 130 ° C a teplota dekarboxylácie je 166 - 180 ° C. Pri kontakte s horúcimi povrchmi alebo ohňom sa kyselina šťaveľová rozkladá a tvorí kyselinu mravčiu a oxid uhoľnatý. Prudko reaguje so silnými oxidačnými činidlami, čo predstavuje nebezpečenstvo požiaru a výbuchu. Reaguje s určitými zlúčeninami striebra za vzniku výbušných oxalátov striebra.
Výroba kovov vzácnych zemín je priemysel, ktorý spotrebúva najväčšie objemy kyseliny šťaveľovej. Podľa štatistík je na výrobu 1 tony kovu vzácnej zeminy potrebná 1 tona kyseliny šťaveľovej. Druhým najväčším spotrebiteľom je farmaceutický priemysel. Celkový podiel spotreby v uvedených dvoch sektoroch predstavuje 68% celosvetovej spotreby kyseliny šťaveľovej.
Kyselina šťaveľová sa okrem toho používa v náterovom priemysle (ako katalyzátor na vytvrdzovanie štiepnych povlakov); v systémoch čistenia vody (chemická metóda čistenia a znižovania tvrdosti vody, čistenie chladív v jadrových elektrárňach); v chemickom priemysle (organická syntéza, výroba plastov, tlačiarenských farieb, syntéza farbív ako súčasť pyrotechnických kompozícií); v chemickej metalurgii (ako súčasť zmesí na čistenie kovov od hrdze, vodného kameňa, oxidov); v analytickej chémii (ako zrazenina prvkov vzácnych zemín); v mikroskopii (ako bielidlo rezov); na výrobu syntetických detergentov (ako bieliace a dezinfekčné prostriedky, prostriedky na čistenie a odstraňovanie močového kameňa, tvrdých solí a hrdze); v textilnom a kožiarskom priemysle (morenie sieťotlačou a farbenie vlny a hodvábu, pri činení koží).

Lakovanie alebo oxidácia ocele je proces vytvárania tenkého jemne kryštalického a jemne pórovitého filmu oxidu na povrchu oceľových častí. Modrením ocele sa usmrtia dva vtáky jedným kameňom: diely získajú esteticky krásny vzhľad a získajú celoživotnú ochranu proti korózii.
Kyselina šťaveľová je súčasťou elektrolytu na leštenie ocele. Charakteristickým znakom leštenia kyselinou šťaveľovou je modro-čierna farba výsledného filmu oxidu. Elektrolyt pozostáva iba z vody a kyseliny šťaveľovej. Na 100 kg vody sa použije 0,3 kg kyseliny šťaveľovej.
Elektrolytické leštenie ocele sa vykonáva pod vplyvom elektrického prúdu s hustotou 1-1,5 A / dm 2, napätie 6-8 V. Teplota roztoku elektrolytu v prevádzkovom režime 25 ° C. Čas spracovania je 90 - 100 minút. Ako anóda sa používa vodiaca doska, ktorej plocha je 1,5-krát väčšia ako plocha časti. Po oxidácii sa dielec spracuje sušením pri teplote 100 - 110 ° C.

Anodická oxidácia hliníka je proces výroby oxidového filmu na hliníku chemicky alebo elektrochemicky z roztokov kyselín a zásad.
Pri eloxovaní v elektrolyte kyseliny šťaveľovej sa získajú filmy, ktoré majú dobré elektrické izolačné vlastnosti. Sú nepriehľadné, maľované ozdobnými zlatými tónmi. V tomto elektrolyte je možné spracovávať zliatiny hliníka s obsahom až 5% medi alebo 4% kremíka. Eloxovanie sa vykonáva jednosmerným alebo striedavým prúdom. Anodizácia pomocou DC sa vykonáva v elektrolyte 3 až 5 kg kyseliny šťaveľovej na 100 kg vody. Prevádzkový režim: teplota elektrolytu 15 - 25 ° C, anódová prúdová hustota 1 - 2 A / dm 2, napätie na kúpeli 40 - 60 V (na konci elektrolýzy dosiahne 60 - 70 V). Aby sa získali pevné filmy s dobrými elektrickými izolačnými vlastnosťami, ich hrúbka by mala byť najmenej 25-40 mikrónov. Škodlivé nečistoty, ktoré zhoršujú kvalitu eloxovania, sú chlór a hliník. Ich prípustná koncentrácia v elektrolyte je 0,04 g / la 30 g / l.

Bielenie dreva sa zvyčajne vykonáva pred farbením, aby sa odstránili škvrny, aby sa získal ľahší povrch. Po bielení je drevo rovnomernejšie a čistejšie.
Kyselina šťaveľová (10% roztok) sa nanáša na bielený povrch, vopred zvlhčený 20% roztokom hydrogensiričitanu sodného. Po nie viac ako 5 minútach sa aplikované formulácie premyjú čistou vodou.
Pre ľahké druhy - lipu, brezu, javor, topoľ - sa odporúča roztok kyseliny šťaveľovej (1,5 - 6 kg) vo vriacej vode (100 kg).
Na zrýchlené bielenie môžete použiť nasledujúce zloženie (kg): kyselina sírová - 20; kyselina šťavelová - 15; peroxid sodný - 25 (alebo peroxid vodíka - 10); voda - 1000.

Kyselina šťaveľová ľahko odstraňuje riasy, mäkkýše, mušle, vápno, hrdzu z podvodnej časti plavidla, motor, hriadeľ. Na tento účel sa jednoducho aplikuje a chvíľu sa ponechá. Potom umyte vodou.
Kyselina šťaveľová ľahko odstraňuje perzistentné znečisťujúce látky, ako sú prach, čierne škvrny oxidových škvŕn (na duralových lodiach), hrdza a motorový olej, vodný kameň z povrchu gélového povlaku, plasty, kovy a lakované povrchy. Drevená lodná kyselina šťaveľová chráni pred plesňou.

Je to účinný prostriedok proti varroatóze včiel v včelínoch (choroba včiel s kliešťom Varroa). Smrť včiel a kráľovien po liečbe sa nepozoruje.
Spracovanie sa vykonáva raz pomocou špeciálne pripraveného roztoku metódou polievania včiel v medzipamäťových priestoroch rýchlosťou 5 ml roztoku na ulicu.
Pripravený pracovný roztok sa môže pripraviť jedným z dvoch spôsobov:
1) zmiešaním 100 g cukru, 100 ml vody a 7,5 g kyseliny šťaveľovej (GOST 22180-76) až do úplného rozpustenia. Akaricídna účinnosť jednej liečby kyselinou šťaveľovou je 85% štyri dni po liečbe.
2) kyselina šťaveľová v koncentrácii 3,75%, použitá v 20% sirupu. Účinnosť spracovania včelstiev s kyselinou šťaveľovou je 95% a nie je nižšia ako účinnosť bivaru (92%).
Ekonomický účinok použitia kyseliny šťaveľovej na zalievanie včiel v medzirámovom priestore v porovnaní s ošetrením bivarom, ktorý má rovnaký spôsob použitia, je spôsobený rozdielom v nákladoch na prípravky, ako aj skutočnosťou, že kyslé ošetrenie sa vykonáva bivarom raz a dvakrát. Celkové náklady na jedno ošetrenie kyselinou šťaveľovou sú menšie ako dvojité ošetrenie bivarom viac ako dvojnásobne (pri zohľadnení mzdových nákladov, cukru a kyseliny).
Kyselina šťaveľová je vysoko účinný ekologický spôsob boja proti varroatóze. Pokiaľ ide o akaricídnu účinnosť, nie je nižšia ako bipín a bivar odporúčaný na toto obdobie. Ošetrenie kyselinou šťaveľovou týmto spôsobom nemá nepriaznivý vplyv na včelské kolónie. Použitie kyseliny šťaveľovej môže zlepšiť hygienickú kvalitu výsledných produktov.
![]()
Kyselina šťaveľová dobre čistí kovy a spóry zo železa, zinku, medi. Zachováva farbu a kov. Kyselinu oxalovú používajú pracovníci múzea a archeológovia na čistenie mincí, spôn, prilieb, kaziet, jedál a oveľa viac.
Na čistenie sa používa 5% roztok kyseliny šťaveľovej (50 gramov na 1 liter). V závislosti od stavu predmetu - čistenie kyselinou šťaveľovou trvá 20 - 40 minút v teplom roztoku a až 3 dni v studenom roztoku. Najčastejšie používajú plastovú nádobu s vyhrievaním vo vodnom kúpeli. Schopnosť použitého roztoku kyseliny šťaveľovej časom reagovať. Závisí to od množstva oxidov odstránených v roztoku.

Tvrdosť vody závisí od množstva solí vápnika a horčíka. Kyselina šťavelová reaguje s týmito soľami. Produkty tejto reakcie sa vyzrážajú.
Zmäkčená voda nesolizuje pôdu a zvyšuje úrodu ovocia a zeleniny, zlepšuje vývoj izbových rastlín.
Na zmäkčenie vody sa použije 1% roztok kyseliny šťaveľovej (10 gramov na 1 liter). Pri izbovej teplote stačí jeden deň na kal. Voda sa stane priehľadnou. Potom sa zrazenina oddelí. Za týmto účelom opatrne vypustite vodu. Kal so soľami nie je nebezpečný, ale nepodlieha ďalšiemu použitiu na farme.
Kyselina šťaveľová je silná kyselina, ktorá v tuhej forme alebo v koncentrovaných roztokoch môže spôsobiť popáleniny pokožky, očí alebo slizníc; dokonca nízke koncentrácie kyseliny šťaveľovej (5 až 10%) pri dlhodobej expozícii sú dráždivé. Boli hlásené prípady úmrtia po požití len 5 g kyseliny šťaveľovej. Príznaky otravy sa objavujú rýchlo: šok, kolaps, kŕče. V takýchto prípadoch sa pozoruje poškodenie obličiek so zrážaním oxalátu vápenatého v obličkových kanáloch. Kŕče môžu byť dôsledkom hypokalcémie. Dlhodobé vystavenie pokožky roztokom kyseliny šťaveľovej alebo draselnej šťaveľovej spôsobuje lokálnu bolesť, cyanózu v prstoch a dokonca aj gangrenózne zmeny. Je zrejmé, že je to kvôli lokálnej absorpcii kyseliny šťaveľovej, čo vedie k artritíde. Chronické systémové choroby spôsobené inhaláciou prachu kyseliny šťaveľovej sú mimoriadne zriedkavé, hoci literatúra opisuje prípad, keď osoba vystavená horúcim výparom kyseliny šťaveľovej (pravdepodobne obsahujúca aerosól kyseliny šťaveľovej) mala príznaky, ako je strata hmotnosti a chronický zápal horných dýchacích ciest. , Z dôvodu silného kyslého účinku kyseliny šťaveľovej by sa mal jej obsah vo vzduchu v priemyselných priestoroch starostlivo monitorovať a nemal by prekročiť koncentrácie, ktoré sú bezpečné pre zdravie.
V priemysle sa kyselina šťaveľová získava oxidáciou uhľohydrátov, alkoholov a glykolov zmesou HN03 a H2S04 v prítomnosti V205 alebo oxidáciou etylénu a acetylénu HN03 v prítomnosti PdCl2 alebo Pd (N03) 2 a tiež oxidáciou propylénu kvapalinou. NO 2.
Federálna agentúra pre vzdelávanie
Štátna vzdelávacia inštitúcia vyššieho odborného vzdelávania
TECHNICKÁ UNIVERZITA V OBLASTI VOLGOGRADU
(Vstu)
Oddelenie "Technológia vysokomolekulárnych a vláknitých materiálov"
Semestrálna práca
disciplína "Základy chemických procesov"
Téma: „Charakterizácia procesov prebiehajúcich pri syntéze kyseliny šťaveľovej. Výpočet materiálovej a tepelnej bilancie. ““
Volgograd 2011
Chemické vlastnosti.
Fyzikálne vlastnosti.
Metódy získavania.
prihláška
Predajný trh
GOST na predaj
Materiálová bilancia
Tepelná bilancia
Chemické vlastnosti:
Kyselina šťaveľová (kyselina etándiová) C2H204 je nasýtená dibázická karboxylová kyselina. Patrí medzi silné organické kyseliny. Má všetky chemické vlastnosti charakteristické pre karboxylové kyseliny. Soli a estery kyseliny šťaveľovej sa nazývajú oxaláty. V prírode sa vyskytuje v šťave a niektorých ďalších rastlinách vo forme oxalátov draslíka a vápnika.
Kyselina šťaveľová bola prvýkrát syntetizovaná v roku 1842 nemeckým chemikom Friedrichom Wöhlerom z tiziana. Kyselina šťavelová (alebo oxalátový ión C204-2) je redukčné činidlo (odfarbuje roztok KMnO4).
Kyselina šťaveľová je ľahko rozpustná vo vode a alkohole. Jedná sa o pomerne silnú organickú kyselinu (trieda nebezpečnosti 3), NOOS-COOH, sú bezfarebné hygroskopické kryštály, ľahko rozpustné vo vode, obmedzene v etylalkohole a dietyléteri, nerozpustné v chloroforme, petroléteri a benzéne. Vytvára dihydrát zmesi C2H204 * 2H20. Horľavá látka v usadenom stave, nebezpečenstvo požiaru. Má silný dráždivý účinok na pokožku, sliznice očí a horné dýchacie cesty.
Kyselina šťaveľová má chemické vlastnosti charakteristické pre karboxylové kyseliny a tvorí dva rady derivátov. Soli a estery kyseliny šťaveľovej sa nazývajú oxaláty. Kyselina šťaveľová tvorí kyslé a stredné estery, amidy, chlorid kyseliny.
Kyselina šťaveľová sa nachádza v šťave a rebarbore ako oxalát draselný.
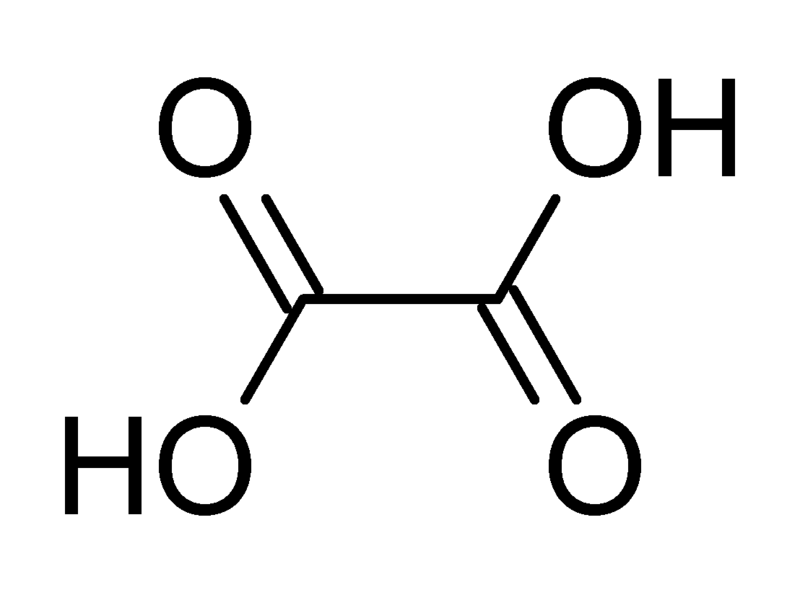
Táto kyselina je v rastlinnom svete veľmi bežná - vo forme solí sa nachádza v listoch šťavy, kyseliny, rebarbory, atď. Soli a estery tejto kyseliny majú triviálne pomenovanie - oxaláty (z gréckeho „Oxalis“ - šťaveľ).
vykazuje podobné vlastnosti kyselín. pretože má funkčnú karboxylovú skupinu. Reakcia tvorby solí dokazuje kyslé vlastnosti kyseliny mravčej. V tomto prípade sa tvoria soli - mravčany.
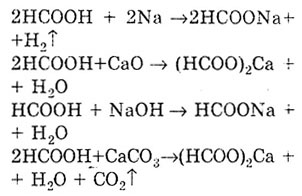
Podobne ako všetky karboxylové kyseliny, aj kyselina mravčia tvorí estery.
Esterifikačná reakcia:
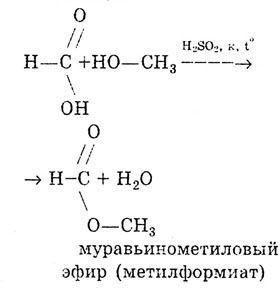
Kyselina mravčia sa líši od ostatných karboxylových kyselín tým, že karboxylová skupina v nej nie je viazaná na uhľovodíkový radikál, ale na atóm vodíka. Kyselina mravčia sa preto môže považovať za kyselinu aj za aldehyd:
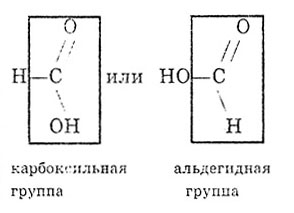
Podobne ako aldehydy môže kyselina mravčia oxidovať:
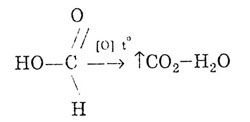
Kyselina mravčia dáva reakciu „strieborného zrkadla“:
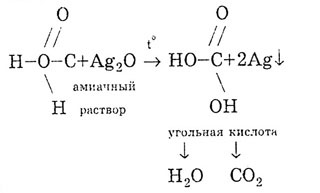
Kyselina mravčia sa pri zahrievaní rozkladá:
![]()
kyselina mravčia patrí do homológnej série monobázických karboxylových kyselín
Fyzikálne vlastnosti:
Teplota sublimácie: pozri poznámky ° C
Teplota topenia: 102 ° C
Relatívna hustota (voda \u003d 1): 1,7
Rozpustnosť vo vode, g / 100 ml: 10
Tlak pár, Pa pri 30 ° C: pozri poznámky
Relatívna hustota pár (vzduch \u003d 1): 3.1
Kyselina šťaveľová je jednou z najsilnejších karboxylových kyselín, ktorá je oveľa silnejšia ako jej homológy.
Kyselina etándová má redukčné vlastnosti: v okyslenom roztoku manganistanu draselného sa oxiduje na oxid uhoľnatý (IV) a vodu.
Pri zahrievaní v prítomnosti kyseliny sírovej dochádza k dekarboxylácii a získa sa oxid uhoľnatý (IV) a kyselina mravčia.
Teploty varu mastných kyselín s normálnou štruktúrou sa prirodzene zvyšujú so zvyšujúcim sa počtom atómov uhlíka. Zistilo sa, že kyslé molekuly sú asociované rovnakým spôsobom, ako sú asociované molekuly vody alebo alkoholu. Nižšie kyseliny sa dobre destilujú vodnou parou, preto sa zvyčajne nazývajú prchavé mastné kyseliny.
Všeobecne sa tiež zvyšujú teploty topenia monobázických kyselín so zvýšeným počtom atómov uhlíka v ich molekulách; súčasne sa však pozoruje nasledujúca pravidelnosť: kyseliny s normálnym reťazcom, ktoré majú párny počet atómov uhlíka, sa zvyčajne topia pri vyššej teplote ako predchádzajúce a nasledujúce členy homológnej série, ktoré majú nepárny počet atómov uhlíka.
CHEMICKÉ NEBEZPEČENSTVO:
Látka sa pri rýchlom zahrievaní nad 150 ° C rozkladá za vzniku toxického plynu. Vodný roztok je kyselina strednej sily, ktorá prudko reaguje so silnými zásadami. Prudko reaguje s oxidačnými činidlami, čo vedie k nebezpečenstvu požiaru a výbuchu. Reaguje so striebrom a vytvára výbušné produkty.
Aplikácie.
Kyselina šťaveľová a jej soli sa používajú v textilnom a kožiarskom priemysle ako moridlo; ako súčasť anódových kúpeľov na nanášanie povlakov Al, Ti a Sn; ako činidlo v analytickej a organickej chémii; zložka zmesí na čistenie kovov od hrdze a oxidov; na ukladanie vzácnych zemín. Oxamid je stabilizátor dusičnanov celulózy, cyan je reakčné činidlo v organickej syntéze, oxalylchlorid je chloračné, chlórkarbonylačné a sieťovacie činidlo v organickej syntéze. Ako celulózové rozpúšťadlá sa používajú dialkyl oxaláty, najmä dietyloxalát a dibutyloxalát; niektoré estery kyseliny šťaveľovej a substituovaných fenolov - ako chemiluminiscenčné činidlá.
Kyselina šťaveľová sa používa na leštenie kovov, v drevospracujúcom priemysle, na čistenie uránu
Oblasti použitia kyseliny šťaveľovej a jej solí (šťaveľany):
v chemickom priemysle (organická syntéza, výroba plastov, tlačiarenských farieb, syntéza farbív ako súčasť pyrotechnických kompozícií);
v chemickej metalurgii (ako súčasť zmesí na čistenie kovov od hrdze, vodného kameňa, oxidov);
v analytickej chémii (ako zrazenina prvkov vzácnych zemín);
v mikroskopii (ako bielidlo rezov);
v textilnom a kožiarskom priemysle (morenie sieťotlačou a farbenie vlny a hodvábu, pri činení koží);
na výrobu syntetických detergentov (ako bieliace a dezinfekčné prostriedky, prostriedky na čistenie a odstraňovanie močového kameňa, tvrdých solí a hrdze);
v kozmetike (ako aktívna prísada pri bielení krémov a krémov z pihy);
v systémoch čistenia vody (chemická metóda čistenia a znižovania tvrdosti vody, čistenie chladív v jadrových elektrárňach);
v medicíne a farmaceutických výrobkoch.
Spôsoby získania:
1) Ako vedľajší produkt pri výrobe kyseliny octovej oxidáciou butánu v kvapalnej fáze.
2) Oxidácia metanolu:
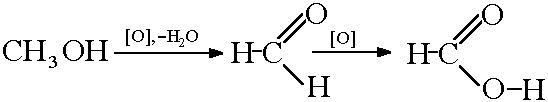
Reakcia oxidu uhoľnatého s hydroxidom sodným:
NaOH + CO-\u003e HCOONa- (+ H3SO4, -Na2SO4) HCOOH
Toto je hlavný priemyselný postup, ktorý sa uskutočňuje v dvoch stupňoch: v prvom stupni sa oxid uhoľnatý pod tlakom 0,6 až 0,8 MPa nechá prechádzať hydroxidom sodným zahriatym na 120 až 130 ° C; v druhom stupni sa na mravčan sodný pôsobí kyselinou sírovou a produkt sa destiluje vo vákuu.
Rozklad glycerolesterov kyseliny šťaveľovej. Za týmto účelom sa zahrieva bezvodý glycerín s kyselinou šťaveľovou, zatiaľ čo voda sa oddestiluje a vznikajú estery kyseliny šťaveľovej. Pri ďalšom zahrievaní sa estery rozkladajú, uvoľňujú oxid uhličitý a vytvárajú sa estery kyseliny mravčej, ktoré po rozklade s vodou poskytujú kyselinu mravčiu a glycerín.
| Súvisiace články: | |
|
Interiér, výzdoba, skladovanie, domáci nápad, škandinávsky štýl, kôš, pletený kôš, háčkovanie, kutilstvo, ručne robené, interiér, výzdoba, pletené, pletenie box
Čoskoro príde leto a podelí sa s nami o všetko, čo má: ... Kyselina šťaveľová: čo o nej vieme
Ahoj všetci! Mnoho ľudí vie, že kyselina šťaveľová spôsobuje tvorbu ... Čo je to startup a kto sú startupy - ako vytvoriť s minimálnymi investíciami a príkladmi najúspešnejších
Preklad Táto príručka je rad klasických príspevkov považovaných za ... | |